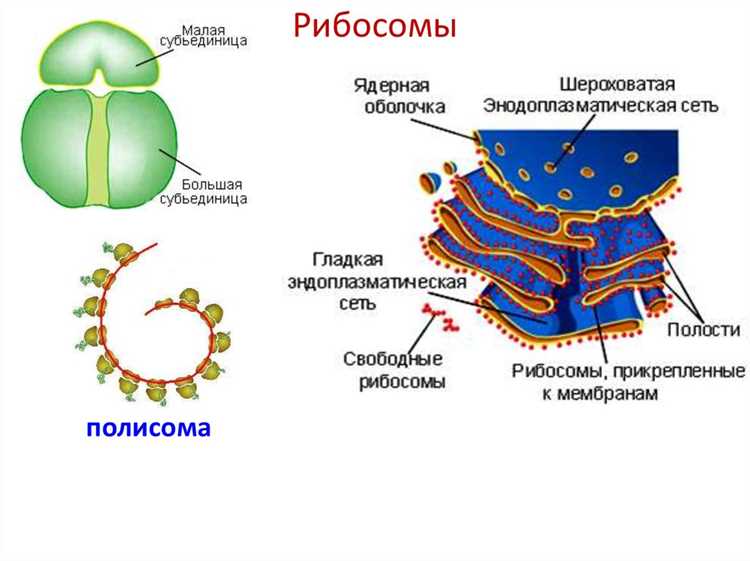
Маленькие, но удивительно сложные структуры, каждая из которых представляет собой фабрику по производству белков, имеют множество функций и работают без усталости. Эти компонентные системы не только служат катализаторами биохимических процессов, но и задействованы в считывании информации, закодированной в молекулах РНК. Каждый размер, форма и местоположение в цитоплазме определяют их специфических функции и взаимодействия.
Видимый под электронным микроскопом, данный элемент образует органеллы, сосредоточенные в рибосомальной небольшом объеме, что позволяет клетке быть высоко организованной и адаптивной. Их способность к сборке аминокислот в полипептидные цепи демонстрирует сложность и универсальность молекулярных механизмов, которые поддерживают жизнь. Активно участвуя в синтезе белков, они обеспечивают функционирование всех клеточных процессов и ткани.
Существуют различные типы указанных структур, находящихся как в свободном состоянии, так и связанных с мембранами эндоплазматического ретикулума. Эти различия определяют не только механизмы синтеза, но и специфику экспортируемых белков и их предназначение. Оценка соединений между производимыми веществами и их целевыми функциями составляет основу для дальнейших исследований в области клеточной биологии и биохимии.
Структура рибосом и их состав
Строение рибосом различается в зависимости от типа организма. У прокариотов они имеют меньший размер по сравнению с эукариотами. Прокариотическая рибосома составляет около 70S (сайберов), в то время как ее эукариотический аналог достигает примерно 80S. Эти единицы обозначают скорость седиментации в центрифуге, что не всегда прямо соотносится с размером или массой.
Основными компонентами рибосом являются рибосомная РНК (рРНК) и рибосомные белки. В структуре эукариотических рибосом можно выделить две субчасти: большая суббелковая (60S) и малая субчасть (40S). Первая включает три молекулы рРНК, а вторая – одну. Прокариотические рибосомы состоят из двух субчастей: 50S и 30S, содержащих соответственно две и одну молекулы рРНК.
Ключевое значение имеет рРНК, так как она обеспечивает каталитическую активность рибосом, способствуя образованию пептидных связей между аминокислотами. Молекулы рРНК обладают структурными и функциональными свойствами, необходимыми для сборки белков на основе мРНК. Кроме того, рибосомные белки, которые входят в состав рибосом, обеспечивают стабильность и корректное функционирование рибосом.
Сочетание рРНК и белков образует сложные структуры, которые можно визуализировать с помощью криоэлектронной микроскопии. Эти технологии позволили детализировать положение рРНК и белков в рибосомах, что способствовало пониманию процесса трансляции.
Совместная работа всех компонентов обеспечивают высокую точность при синтезе белков, что делает данную структуру ключевым игроком в биохимических процессах. Эффективное взаимодействие между субчастями рибосом и мРНК определяет скорость и качество биосинтеза полипептидов.
Типы рибосом: прокариоты и эукариоты
Существуют два основных типа рибосом, которые различаются по своим характеристикам в прокариотах и эукариотах. Эти различия определяют особенности синтеза белка и биохимические процессы в организмах.
Прокариотические структуры имеют размер, примерно равный 70S, где S обозначает скорость седиментации. Они сочетают в себе две субъединицы: большую (50S) и малую (30S). Формирование белков происходит непосредственно в цитоплазме, так как пространство вокруг структур ограничено. Эти единицы способны синтезировать белки быстро, что важно для выживания прокариотических клеток.
В эукариотах рибосомы значительно крупнее – размер составляет около 80S, также состоящие из двух субъединиц: 60S и 40S. Эти структуры могут находиться как в цитоплазме, так и на мембране эндоплазматического ретикулума, что обеспечивает регулирование синтеза различных типов белков, включая секретируемые и мембранные. Сложность организации указывает на уровне контроля и разнообразия функции.
Параметрическая разница между типами также отражает состав рибосомных РНК и белков. Прокариотические структуры содержат 16S рРНК в малой субъединице и 23S рРНК в большой, тогда как в эукариотах эта составляющая включает 18S и 28S соответственно. Эти особенности влияют на чувствительность к антибиотикам и возможности применения лекарств в медицине.
Возможность различить типы рибосом по их структуре и составу рРНК полезна при изучении эволюции и классификации живых организмов. Наличие этих отличий помогает специалистам в подбирании методов, направленных на более глубокое понимание клеточных механизмов и разработки новых терапий.
Процесс биосинтеза белка на рибосомах
После формирования инициационного комплекса происходит этап элонгации. Этот процесс подразумевает последовательное присоединение аминокислот к растущей полипептидной цепи. Каждая тРНК, обладая специфическими антикодонами, транспортирует соответствующие аминокислоты, которые соединяются пептидными связями под действием ферментов, находящихся в рибосомах.
Важным аспектом элонгации является механизм транслокации. После добавления каждой аминокислоты, рибосома перемещается вдоль мРНК, освобождая активный сайт для следующей тРНК. Этот цикл продолжается, пока не достигнется стоп-кодон, что сигнализирует о завершении синтеза полипептида.
Завершение включает образование полипептида, который затем подвергается посттрансляционным модификациям. Эти изменения могут включать гликозилирование, фосфорилирование и другие модификации, определяющие функциональные свойства белка.
Для повышения точности и скорости синтеза, организм использует множество макромолекул и факторы, которые участвуют в каждом из этапов. Корректное взаимодействие всех компонентов обеспечивает синтез функциональных белков, необходимых для жизнедеятельности.
Функции рибосом в клеточном метаболизме
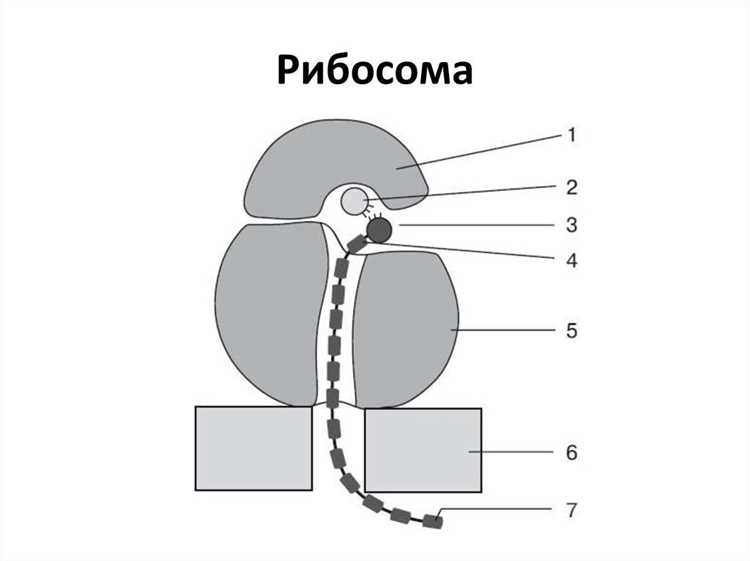
Процесс синтеза белков происходит на малых структурах, отвечающих за перевод информации, закодированной в молекулах РНК, в аминокислотные последовательности. Этот механизм включает комплексные взаимодействия между различными молекулами, обеспечивающими не только сборку полипептидных цепей, но и контроль за качеством синтезируемых белков.
Каждая такая единица взаимодействует с мРНК, считывая ее последовательности и обеспечивая точное выполнение инструкции. Аминокислоты, поставляемые транспортными РНК, соединяются в специфических местах, благодаря чему образуются пептидные связи. В этом процессе критически важна правильная компоновка, так как даже небольшие ошибки могут приводить к функциональным сбоям.
Кроме того, определенные структуры участвуют в процессе посттрансляционной модификации растущих полипептидных цепей, что позволяет окончательным продуктам достигать требуемой конфигурации и выполнять свои функции в метаболических процессах. Существует также наличие специализированных форм, которые обеспечивают синтез белков, необходимых для функции мембран и органелл.
Производя различные белковое соединения, эти структуры также играют значимую роль в клеточной реакции на стрессовые факторы, таких как изменения температуры или наличие токсичных веществ. Быстрый синтез специфических белков адаптации позволяет организму выживать в неблагоприятных условиях.
Совместная работа с молекулами шаперонов, обеспечивающих правильную сборку и сворачивание, дополняет функциональные возможности, тем самым способствуя поддержанию метаболического равновесия и обеспечивая клеточный гомеостаз. В этом аспекте структуры выступают в качестве ключевых игроков, обеспечивая неуклонное выполнение жизненно важных процессов.
Функционирование рибосом в ответ на стрессовые условия
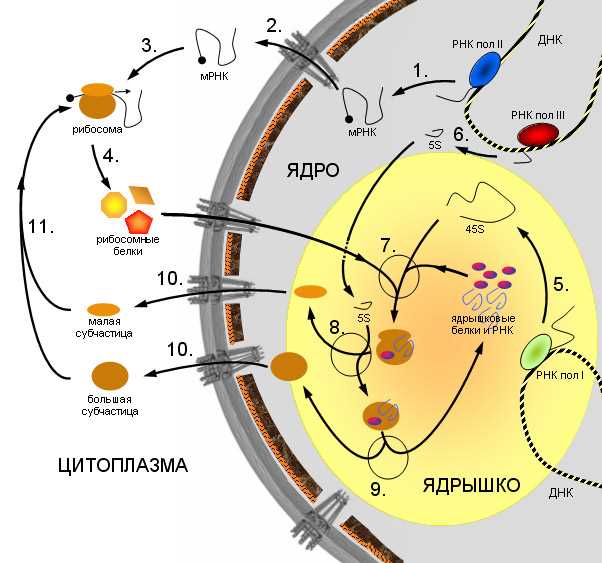
В условиях стресса, клеточные структуры адаптируются для поддержания гомеостаза. В этом процессе активируется синтез белков, который играет ключевую роль в восстановлении энергетического баланса. На этом этапе происходит перераспределение ресурсов с акцентом на защитные и восстановительные механизмы.
Изменения в концентрации специфических мРНК являются одним из первых признаков стрессового ответа. Эти молекулы направляют синтез белков с функциями, способствующими выживанию, например, шаперонов и антиоксидантов. К примеру, в условиях оксидативного стресса повышается уровень мРНК, кодирующих супероксиддисмутазу, что позволяет снизить уровень свободных радикалов.
Также наблюдается активация сигнальных путей, таких как путь рКК-AMP, который инициирует транскрипцию генов, ответственных за восстановление клеток. На этапе трансляции происходит уникальная модификация рибосом, что увеличивает их аффинность к определенным мРНК.
Чем выше уровень стресса, тем большее внимание уделяется селективному синтезу белков. Клетки могут переключаться на использование резервных запасов мРНК, которые ранее находились в неактивном состоянии. Этот механизм гарантирует быструю адаптацию к изменяющимся условиям.
Идентификация мишеней для терапевтического воздействия в области защиты от стресса имеет значительное значение. Например, ингибиторы специфических путей могут препятствовать чрезмерной активности, приводящей к клеточной гибели.
Знание о том, как клетки регулируют уровень белкового синтеза в ответ на стресс, открывает перспективы для разработки лечебных стратегий при различных заболеваниях, связанных со стрессом. Такие вмешательства могут стать основой для создания целевых терапий, направленных на коррекцию ошибок в регуляции белкового синтеза.
Влияние антибиотиков на рибосомы
Разные группы антибиотиков нацелены на определенные стадии производства белков. Например, аминогликозиды, такие как гентамицин, связываются с малой субъединицей, что приводит к ошибкам в считывании мРНК и производству ненормальных белков. Это вызывает повреждение целостной системы жизнедеятельности бактерий.
Тетрациклины блокируют взаимодействие ацилтРНК с рибосомами, что полностью прерывает процесс трансляции. Благодаря этому механизм у микробов останавливается, что делает их невыносимыми для дальнейшего размножения.
Макролиды, включая эритромицин, воздействуют на трансляцию, связываясь с большой субъединицей и нарушая перемещение мРНК. Это приводит к сбоям в синтезе белков. В результате такое влияние отслеживается в снижении вирулентности и торможении роста бактериальных популяций.
| Группа антибиотиков | Механизм действия | Примеры |
|---|---|---|
| Аминогликозиды | Увеличение ошибок в считывании мРНК | Гентамицин, Тобрамицин |
| Тетрациклины | Блокада связывания ацилтРНК | Доксициклин, Тетрациклин |
| Макролиды | Нарушение перемещения мРНК | Эритромицин, Азитромицин |
Причины побочных эффектов при использовании антибиотиков также связаны с тем, что они могут оказывать влияние на целевые структуры млекопитающих, что ведет к нарушению синтеза белков. Этот аспект требует тщательного выбора препаратов и контроля за их применением для избежания необратимых последствий.
Методы исследования рибосом в молекулярной биологии
Современные подходы к изучению этого жизненно важного компонента клеток включают несколько методик, каждая из которых обладает своими преимуществами.
- Композиционная анализ: Используется для определения белкового состава. Применение масс-спектрометрии позволяет идентифицировать полипептидные цепи и их модификации, что важно для понимания функций отдельных компонентов.
- Электронная микроскопия: Высокая разрешающая способность позволяет получать детализированные изображения объектов. Крио-электронная микроскопия помогает визуализировать структуры в естественном состоянии, обеспечивая более достоверные результаты.
- Кристаллография рентгеновскими лучами: Эта методика используется для определения трехмерной структуры на молекулярном уровне. Позволяет выявлять взаимосвязи между структурой и функцией подструктур.
- ППЦ-технологии (полифункциональная протеомика): Упрощает анализ взаимодействий между различными белками и другими молекулами. Методы, такие как CO-IP и Y2H, позволяют изучать взаимодействия в контексте целых комплексов.
- Методы анализа РНК: Структурный анализ рибонуклеиновых кислот с использованием нуклеаз и других ферментов позволяет определить, какие участки участвуют в сборке и функционировании молекул.
- Геномное редактирование: Использование CRISPR/Cas9 для модификации генов, кодирующих рибосомные белки, обеспечивает понимание, как изменения в генетическом материале влияют на синтез.
Эти методы предоставляют разнообразные инструменты для глубокого анализа и раскрытия функций этих молекул, важнейших для жизнедеятельности клеток. Интеграция нескольких подходов способствует комплексному пониманию их значимости.
Будущее изучения рибосом и их применение в биотехнологиях
С развитием молекулярной биологии открываются новые горизонты в понимании структуры и функции этих микроскопических комплексов. Применение методов кристаллографии и ядерного магнитного резонанса позволит получить более детальные сведения о молекулярной архитектуре данных объектов.
Современные исследования сосредоточены на следующих направлениях:
- Биосинтез белков: Углубленное изучение механизмов, задействованных в синтезе полипептидных цепей, может привести к созданию новых терапевтических белков для лечения различных заболеваний.
- Генетические технологии: Клонирование генов и использование новейших методов редактирования (например, CRISPR) могут усиливать синтетическую активность, что открывает возможности для производства высокоактивных и специфичных белков.
- Биоинформатика: Моделирование взаимодействий между молекулами позволит предсказать поведение и совместимость различных компонентов, что облегчит разработку инновационных биологически активных веществ.
Основные перспективы внедрения знаний о данных структурах в биотехнологиях:
- Создание новых медикаментов с высокой селективностью и минимальными побочными эффектами.
- Разработка вакцин, которые будут обеспечивать улучшенную защиту против инфекционных заболеваний благодаря оптимизации белковых антигенов.
- Инженерия живых организмов для повышения их устойчивости к стрессовым факторам и улучшения продуктов питания.
Повышенное внимание к данным компонентам приводит к появлению новых методов исследования и их применения в различных областях, включая агрономию, медицину и экологию. Понимание структурных особенностей и функциональных возможностей данных единиц позволит значительно продвинуться в разработке более эффективных технологий в будущем.