Современные исследования в области защитных механизмов организма открывают новые горизонты в понимании того, как живые организмы взаимодействуют друг с другом и с внешней средой. Адаптивные и врожденные механизмы, направленные на поддержание гомеостаза, требуют строгого контроля и координации, чтобы избежать чрезмерного или недостаточного реагирования на патогены. Понимание этих процессов имеет огромное значение, особенно в контексте разработки инновационных терапий и вакцин.
Одним из ключевых аспектов функционирования защитных систем является баланс между различными клеточными типами. Т-лимфоциты, В-лимфоциты и макрофаги взаимодействуют друг с дружкой через сложные молекулы сигнализации, что позволяет обеспечивать точечное поражение опасных агентов. Патологии, возникающие при нарушениях в этих взаимодействиях, подчеркивают важность углубленного изучения клеточной коммуникации и его молекулярной основы.
Специфические факторы, регулирующие активность клеток, такие как цитокины и хемокины, играют решающую роль в формировании и успешном применении ответных реакций. Лабораторные и клинические данные указывают на то, что нарушение баланса между про- и противовоспалительными цитокинами может приводить к возникновению различных заболеваний, включая автоиммунные и аллергические реакции. Владение знаниями о механизмах их действия открывает доступ к новым подходам в терапии.
Интересный аспект заключается в влиянии микробиоты на защитные процессы организма. Исследования показали, что микробы, обитающие в кишечнике, могут оказывать значительное влияние на формирование защитных клеток, тем самым изменяя реакцию организма на инфекцию. Эта связь подчеркивает многофакторность факторов, участвующих в поддержании здоровья и предотвращении заболеваний.
Роль Т-клеток в регуляции адаптивного иммунного ответ
Т-клетки выполняют ключевые функции в активации и поддержании специфической реактивности организма. Главные группы Т-клеток, такие как CD4+ хелперы и CD8+ цитотоксические, активно участвуют в различных механизмах, направленных на устранение чуждых антигенов.
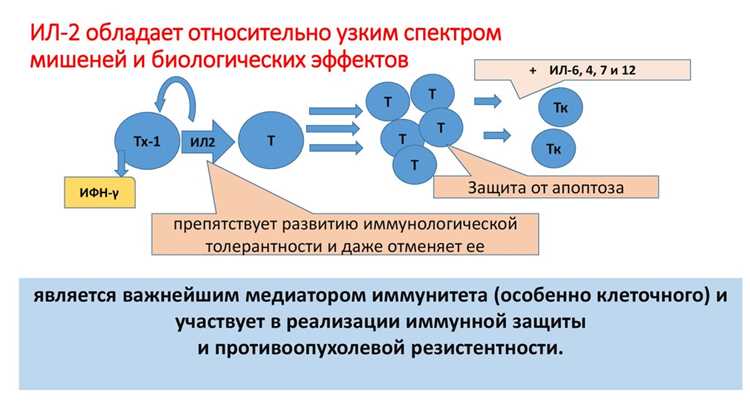
Т-клетки CD4+ играют важную роль в поддержании эфирной среды T-клеточной активации, способствуя дифференцировке других клеток. Они вырабатывают множество цитокинов, таких как IL-2, IL-4 и IFN-γ, которые усиливают функцию B-клеток и макрофагов.
Цитотоксические Т-клетки CD8+ непосредственно уничтожают зараженные клетки, обеспечивая защиту от вирусов и некоторых видов опухолей. Процесс их активации зависит от взаимодействия с антиген-презентирующими клетками (АПК), что приводит к их пролиферации и дифференцировке.
Т-клетки также участвуют в создании иммунной памяти. При повторном контакте с тем же патогеном, память активирует более быструю и мощную реакцию, обеспечивая защиту организма.
Интересно, что Т-клетки могут также выполнять регуляторную функцию, подавляя чрезмерные реакции. Это достигается благодаря выделению цитокинов, таких как IL-10 и TGF-β, что предотвращает аутоиммунные заболевания и гиперчувствительность.
- Т-клетки обеспечивают активную защиту от инфекций.
- Взаимодействие с АПК необходимо для эффективной активности.
- Создание иммунной памяти способствует быстрому реагированию.
- Регуляторные функции защищают от аутоиммунных проявлений.
Таким образом, Т-клетки являются важными участниками сложного процесса, обеспечивающего защиту организма и поддерживающего гомеостаз.
Влияние цитокинов на направление иммунного ответа
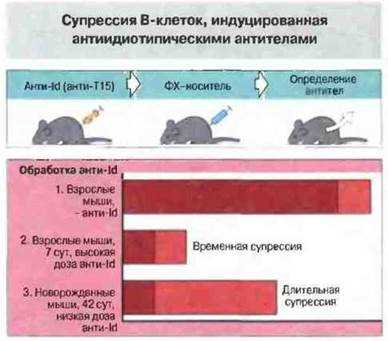
Цитокины представляют собой белки, которые выступают в роли сигнализаторов в клетковом взаимодействии. Их продукция и действие влияют на дифференцировку и активацию клеток, составляющих защитные механизмы организма. Каждый тип цитокина может менять ход реакций иммунной системы, определяя, каким образом подойдут к атакующим патогенам.
Цитокины Th1, такие как интерферон-гамма (IFN-γ), способствуют активации макрофагов и повышают их способности к фагоцитозу и уничтожению микроорганизмов. Это критично для борьбы с внутриклеточными инфекциями, такими как туберкулез или вирусные заболевания.
Наоборот, цитокины Th2, например, интерлейкин-4 (IL-4), играют важную роль в активации В-лимфоцитов, что необходимо для продуктивного ответа на экзо- и бактерии. IL-4 стимулирует синтез антител IgE, что связано с аллергическими реакциями и защитой от гельминтов.
Интерлейкин-6 (IL-6) совмещает функции как Th1, так и Th2 цитокинов. Он отвечает за реакцию острофазовых белков и может поддерживать воспаление. Высокие уровни IL-6 ассоциируются с хроническими воспалительными состояниями, что требует внимания к его регуляции.
Обратите внимание, что цитокины могут действовать как в местной, так и в системной регуляции. Это может быть использовано в терапевтических подходах, например, для активации клеток Т-лимфоцитов в борьбе с онкологическими заболеваниями.
Система цитокинов не статична; один и тот же цитокин может вызывать разные реакции в зависимости от контекста, в котором он выделяется. Поэтому важно учитывать соотношение между различными цитокинами при анализе реакций. Разработка блокаторов или модуляторов отдельных цитокинов позволяет направить защитный механизм на борьбу с конкретными патологиями, что открывает новые горизонты в лечении.
Механизмы действия регуляторных Т-клеток
Регуляторные Т-клетки (Treg) играют ключевую роль в поддержании иммунного гомеостаза, обеспечивая контроль за активностью других клеток. Их функциональные механизмы варьируются и включают как клеточные контакты, так и секрецию растворимых молекул.
Один из основных способов их воздействия связан с выделением цитокинов, таких как IL-10 и TGF-β. Эти молекулы подавляют активность эффекторных клеток, таких как Т-клетки и макрофаги, что приводит к уменьшению воспалительной реакции. IL-10 играет роль в снижении продукции провоспалительных цитокинов, тогда как TGF-β участвует в индуцировании анергии и апоптоза активированных Т-клеток.
Помимо секреции цитокинов, Тreg могут взаимодействовать с другими клетками через прямые клеточные контакты. Например, выражение молекул клеточной адгезии, таких как CTLA-4 и PD-1, позволяет им подавлять активность Т-клеток за счет конкуренции за ко-сталимирующие сигналы. Это приводит к снижению пролиферации и функциональной активности наивных и эффекторных Т-клеток.
Тreg также регулируют функции дендритных клеток. Подавляя их способность активировать Т-клетки, они таким образом влияют на исход иммунного ответа. Дендритные клетки, в свою очередь, могут модифицироваться под влиянием растворимых факторов, выделяемых Тreg, что значительно изменяет их представление антигена и секрецию цитокинов.
Эти клеточные механизмы действуют в органах, таких как лимфатические узлы и селезенка, где Тreg обеспечивают контроль над активацией Т-клеток и границей между защитной реакцией и автоиммунитетом. Эффективность Тreg зависит от их численности и функционального состояния, что, в свою очередь, происходит под влиянием различных факторов, включая микробиоту и питание.
В качестве терапевтической стратегии, нацеленной на Тreg, существуют подходы, включающие расширение этих клеток in vitro для последующего введения пациентам с автоиммунными расстройствами. Также разрабатываются методы, направленные на модификацию активности регуляторных Т-клеток с целью улучшения иммунотерапии в онкологии.
Связь между микробиомом и иммунным ответом
Микробиом человека представляет собой разнообразное сообщество микроорганизмов, которые обитают на поверхности кожи, в кишечнике и других частях организма. Эти микроорганизмы активно участвуют в формировании защитных механизмов и адаптации к внешним воздействиям.
Исследования показывают, что микрофлора кишечника может влиять на развитие аллей и автоиммунных заболеваний, например, при дисбиозе фиксируются изменения в количестве таких бактерий, как Firmicutes и Bacteroidetes. Увеличение числа Firmicutes связано с различными воспалительными процессами, в то время как уровень Bacteroidetes способен модифицировать иммунные реакции.
Пробиотики, содержащие живые штаммы полезных микробов, могут служить способом коррекции микробиома и восстановление баланса флоры. Они помогают снизить уровень провоспалительных цитокинов, таких как интерлейкин-6, что способствует облегчению симптомов аллергических реакций и улучшению состояния при воспалительных заболеваниях.
Рацион, богатый клетчаткой, способствует росту полезных бактерий, таких как Lactobacillus и Bifidobacterium, которые участвуют в выработке короткоцепочечных жирных кислот, обладающих противовоспалительными свойствами. Подобное питание может стать основной стратегией борьбы с хроническими воспалениями и поддержания здоровья.
Недавние исследования показывают, что специфические штаммы микробов могут повышать продукцию антител и активировать T-клетки, тем самым усиливая защитные механизмы. Например, Lactobacillus rhamnosus показал способность модифицировать активность CD4+ T-клеток, что может быть полезным при вакцинации.
Дисбаланс в микробиоме также связан с развитием заболеваний, таких как диабет 1 типа и рассеянный склероз. Наличие определенных бактерий может предрасполагать к аутоиммунным реакциям, и умышленная манипуляция микрофлорой предоставляет новые перспективы для профилактики и лечения.
Роль антигенпрезентирующих клеток в активации иммунного ответа
Антигенпрезентирующие клетки (АПК) играют ключевую роль в инициировании реакции со стороны организма на патогены. К основным типам АПК относятся дендритные клетки, макрофаги и В-лимфоциты, которые обладают способностью улавливать, перерабатывать и представлять антигены Т-клеткам.
Дендритные клетки, как наиболее эффективные АПК, мигрируют из тканей в лимфатические узлы, где происходит активация Т-клеток. Их способность к захвату и обработки антигенов обеспечивает синтез сигналов, необходимых для активации CD4+ и CD8+ Т-лимфоцитов. Это происходит через взаимодействие молекул основного комплекса гистосовместимости (МНС) с TCR (T-клеточный рецептор).
Макрофаги, находясь в тканях, поддерживают процессы фагоцитоза и представления антигенов, играя важную роль в направленности и типе иммунного ответа. Они активируются различными модуляторами, такими как интерлейкин-1 (IL-1) и факторы некроза опухолей (TNF), что усиливает их способность к презентации.
В-лимфоциты не только производят антитела, но также выступают в роли АПК. Они способны захватывать свободные антигены, и после их переработки представляют в форме МНС II, активируя Т-хелперы.
Существуют различные молекулы адгезии и кофакторы, такие как CD28, которые способствуют взаимодействию между АПК и Т-клетками. Эти взаимодействия увеличивают аффинитет рецепторов и повышают активность клеток. Т-лимфоциты, получая сигналы от АПК, начинают пролиферацию и дифференциацию в эффекторные и мемори-клетки.
Правильная презентация антигенов и взаимодействие с Т-клетками являются основополагающими для формирования специфического ответа на инфекции. Изучение механизмов, через которые АПК активируют Т-клетки, открывает новые возможности для вакцинации и иммунотерапии рака, позволяя создавать более целенаправленные и безопасные подходы к лечению. Таким образом, понимание роли АПК имеет прямое отношение к разработке новых стратегий в борьбе с инфекциями и злокачественными образованиями.
Иммунный ответ при аутоиммунных заболеваниях

Аутоиммунные заболевания развиваются, когда организм начинает атаковать собственные клетки, воспринимая их как чуждые. Этот процесс, часто вызванный сбоями в каналах, ответственных за самосознание, приводит к воспалению и повреждению тканей.
- Типы клеток. Важную роль в аутоиммунных реакциях играют Т-кли marginal. Цитотоксические Т-клетки уничтожают задерживающие инфекции через уничтожение клеток, а Т-хелперы координируют другие элементы.
- Цитокины. Эти сигнальные молекулы, такие как интерлейкины и опухолевая некрозная фактор, участвуют в межклеточной коммуникации, усиливая или подавляя воспаление.
- Антитела. Аутоанти тела образуются против собственных белков, что приводит к патологиям, как в случае системной красной волчанки.
Различные механизмы запускают и поддерживают аутоиммунные процессы. Например, инфекционные агенты могут вызывать перекрестную реакцию, что приводит к признанию собственных клеток как врагов.
- Генетическая предрасположенность. Многие аутоиммунные заболевания, такие как рассеянный склероз или диабет 1 типа, имеют наследственные компоненты.
- Экологические факторы. Условия жизни, стрессы и хронические инфекции могут способствовать возникновению этих расстройств.
Эффективное управление аутоиммунными заболеваниями требует индивидуального подхода. Основные стратегии включают:
- Иммуносупрессия. Применение кортикостероидов или биопрепаратов снижает активность иммунной системы.
- Коррекция образа жизни. Диеты, физическая активность и избегание стресса могут снизить симптомы.
- Мониторинг состояния. Регулярные обследования необходимы для оценки состояния и корректировки терапии.
Научные исследования продолжают выявлять новые возможности в борьбе с аутоиммунными заболеваниями, включая применение стволовых клеток и направленную терапию.
Регуляция воспалительных процессов: механизмы и примеры
Воспалительные процессы представляют собой важную часть защитного механизма организма, однако их чрезмерная активность может привести к патологическим состояниям. Основные механизмы контроля воспаления включают секрецию противовоспалительных цитокинов, взаимодействие клеток различных типов и структурные изменения в тканях.
Одним из ключевых игроков в этом процессе является интерлейкин-10 (IL-10), который вырабатывается Т-клетками и макрофагами. Этот цитокин подавляет синтез про-воспалительных молекул, таких как TNF-α и IL-6, осуществляя тем самым корректировку воспалительной реакции. Исследования показывают, что уровень IL-10 снижен при воспалительных заболеваниях, таких как артрит и болезнь Крона.
Транскрипционные факторы, такие как NF-κB, играют центральную роль в активации генов, ответственных за выработку воспалительных медиаторов. Регуляция их активности осуществляется через различные сигнальные пути, включая пути TLR (Toll-like receptors). Примером может служить уничтожение NF-κB через ингибитор IκB, который останавливает его перемещение в ядро клетки. При этом происходит уменьшение экспрессии про-воспалительных генов.
Важным аспектом снижения воспалительной активности служит адекватная работа макрофагов. Эти клетки могут проявлять как про-воспалительные, так и противовоспалительные свойства. В состоянии M1 они производят цитокины, способствующие воспалению, тогда как в состоянии M2 активируют процессы заживления тканей и подавляют воспалительные реакции.
Примеры сравнения различных механизмов представлены в таблице ниже:
| Механизм | Описание | Примеры |
|---|---|---|
| Интерлейкин-10 | Противовоспалительный цитокин, подавляющий активность макрофагов | Сниженный уровень IL-10 при болезни Крона |
| NF-κB | Транскрипционный фактор, активирующий подавляющие воспалительные гены | Ингибирование с помощью IκB |
| Типы макрофагов | Разные фенотипы с различными функциями | M1 (воспаление) и M2 (заживление) |
Участие микробиоты в контроле воспалительных процессов также актуально. Пробиотики могут способствовать повышению уровня противовоспалительных цитокинов, таких как IL-10, и снижению уровня про-воспалительных. Это открывает новые горизонты в профилактике и лечении воспалительных заболеваний кишечника.
Таким образом, понимание механизмов контроля воспалительной активности создает возможность для разработки новых терапевтических подходов и препаратов, направленных на балансировку воспалительной реакции и предотвращение осложнений. Исследования продолжаются, чтобы более глубоко изучить каждую из составляющих данного процесса.
Новые подходы к терапии на основе модуляции функциональности клеток иммунной системы
Препараты, такие как Nivolumab и Pembrolizumab, показывают высокую эффективность в лечении меланомы и не малоклеточного рака легкого. Их применение может увеличить выживаемость пациентов, что подчеркивает важность искусственного вмешательства в механизмы торможения иммунного реагирования.
Кроме того, разработка специфических ингибиторов сигнальных молекул, таких как JAK-STAT, открывает новые горизонты в терапии аутоиммунных состояний. Поскольку активация этого пути приводит к чрезмерному производству провоспалительных цитокинов, целенаправленные ингибиторы могут снизить воспаление и облегчить состояние пациента.
Генетическая модификация клеток, особенно Т-клеток с помощью технологии CAR-T, также привлекает внимание. Данный подход позволяет создать клетки с рецепторами, способными распознавать специфические антигены на опухолевых клетках. Применение CAR-T-клеток демонстрирует обнадеживающие результаты в лечении тяжелых форм лейкемии и лимфомы.
Терапия на основе пробиотиков и пребиотиков как способ повышения активности защитных механизмов организма также становится актуальной. Исследования показывают, что микробиом человека может существенно влиять на реакцию клеток защиты. Введение определенных штаммов бактерий может улучшить общее состояние, усиливая продукцию некоторых цитокинов и активируя фагоцитарные способности макрофагов.
Внедрение методов редактирования генома, таких как CRISPR/Cas9, представляет собой перспективный путь для коррекции генетических дефектов, способствующих развитию болезней. Этот подход демонстрирует потенциал не только в исследовании функций клеток, но и в клинической практике для лечения наследственных заболеваний.
Итак, новые методы терапии нацелены на более глубокое понимание клеточных процессов и позволяют разрабатывать специфические стратегии для борьбы с заболеваниями, повышая шансы на выздоровление и улучшение качества жизни пациентов.
Перспективы исследований в области иммунорегуляции
Клинические испытания показывают, что использование моноклональных антител, направленных на конкретные молекулы, регулирующие защитные реакции, может предоставить новые возможности для терапии аутоиммунных заболеваний и аллергий. Важно сосредоточиться на интерлейкинах и других цитокинах, которые участвуют в активации или угнетении защитных клеток. Разработка маломолекулярных соединений, способных влиять на эти сигнальные пути, может кардинально изменить подход к лечению.
Сравнительный анализ данных на молекулярном уровне из различных популяций также открывает перспективы для индивидуализированной медицины. Понимание генетических и эпигенетических изменений, связанных с защитной функцией, может помочь в разработке персонализированных подходов к терапии. Это требует создания специализированных биобанков и взаимодействия между генетиками, иммунологами и клиницистами.
Исследования клеточной терапии, включая применение стволовых клеток, показывают обнадеживающие результаты в восстановлении функций органов, поврежденных в результате аутоиммунных заболеваний. Вместе с тем, необходимо сосредоточиться на оптимизации методов изоляции и манипуляции клетками, чтобы минимизировать риски и повысить эффективность при использовании таких терапий.
Будущее исследований в этой области связано с интеграцией новых технологий, таких как системы искусственного интеллекта для анализа больших данных. Использование алгоритмов машинного обучения поможет выявлять новые молекулы и пути воздействия, а также оптимизировать существующие терапевтические стратегии.