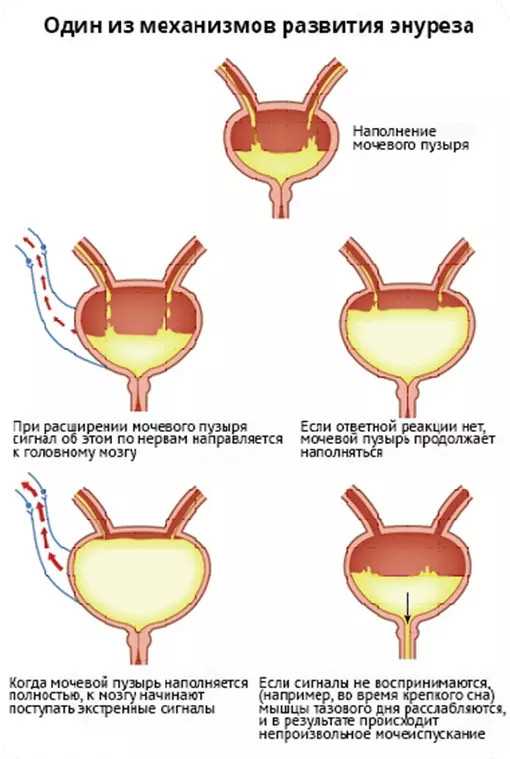
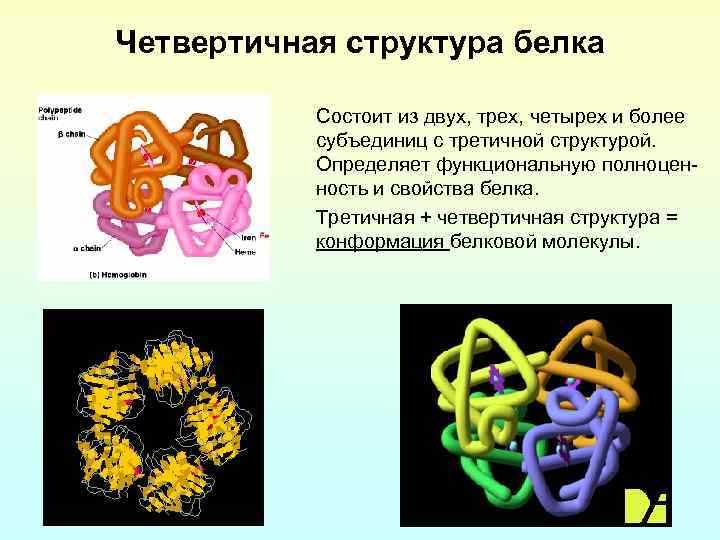
Эти сложные молекулы представляют собой ключевые компоненты живых организмов, их трехмерная конфигурация оказывает значительное влияние на функционирование и взаимодействие внутри клеток. Каждая молекула имеет уникальные черты, определяющие её физико-химические свойства и роли в биологических процессах. Например, спиральные, складчатые и глобулярные формы обеспечивают молекулам способность взаимодействовать с другими соединениями, что критически важно для клеточной активности.
В структуре таких макромолекул наблюдаются определенные организованные элементы, которые влияют на их стабильность и реакционную способность. Альфа-спирали и бета-складки играют важные роли в образовании структурных единиц, а также участвуют в образовании активных сайтов. Специфические взаимодействия между атомами, такие как водородные связи и ионные взаимодействия, формируют прочные связи, обеспечивающие целостность молекулы и её функциональность.
Существует несколько типов соединений, каждый из которых имеет свои характеристики и специальных функций. Например, ферменты в основном представляют собой глобулярные структуры, обеспечивая каталитические процессы, тогда как волокнистые молекулы, такие как коллаген, предоставляют механическую поддержку тканям. Сложные молекулы, обладая разнообразием форм, могут выполнять многочисленные функции, которые являются критически важными для жизни. Понимание этих форм открывает новые горизонты в разработке медикаментов и методов лечения различных заболеваний.
Влияние водородных связей на стабилизацию трехмерной конфигурации
Водородные связи играют важную роль в формировании и поддержании пространственного расположения полипептидной цепи. Эти взаимодействия возникают между атомами водорода, связанными с высокоэлектронегативными элементами, и другими электроотрицательными атомами, что придаёт стабильность структурным элементам.
Каждая водородная связь добавляет дополнительную силу к взаимодействиям между квадратами полипептидной цепи, препятствуя их диссоциации и влияя на общую конформацию. Именно такие взаимодействия влияют на вторичное строение, создавая альфа-спирали и бета-слои, которые затем служат основой для окончательной формы молекулы.
Посмотрим на таблицу, иллюстрирующую влияние водородных связей на формирование высокоорганизованных конформаций:
| Тип взаимодействия | Роль в молекулярной стабильности | Примеры молекул |
|---|---|---|
| Водородные связи | Укрепляют альфа-спирали и бета-слои | Кератин, коллаген |
| Ионные связи | Способствуют общей структурной целостности | Ферменты, мембранные белки |
| Гидрофобные взаимодействия | Скрывают неполярные группы внутри структуры | Мембранные рецепторы |
Варьирование интенсивности водородных связей может существенно влиять на функциональность и активность полипептидов. Существуют некоторые факторы, которые стоит учитывать для оптимизации этой стабильности, такие как pH среды, температура и наличие ко-факторов.
Эти взаимодействия обеспечивают не только хроническую стабильность, но и позволяют белковым молекулам адаптироваться к изменениям во внешней среде. Поддержание водородных связей является ключом к функциональности и жизнеспособности белковых комплексов.
Роль гидрофобных взаимодействий в формировании белковых складок
Гидрофобные взаимодействия представляют собой один из ключевых механизмов, способствующих сворачиванию полипептидных цепей в компактные структуры. Водные среды, в которых белки функционируют, способствуют тому, что неполярные аминокислоты стремятся минимизировать контакт с водой. Этот процесс приводит к образованию стабильных внутренних областей, содержащих эти аминокислоты, что в свою очередь способствует формированию пространственной конфигурации.
При взаимодействии полярных групп воды с неполярными радикалами аминокислот происходит вытеснение воды, что усиливает притяжение между гидрофобными остатками. Наиболее выраженные эффект наблюдается в участках, где много альфа-спиралей и бета-слоев, а также в местах, где соединяются различные мотивы. Эти области играют роль «якорей», объединяющих различные части молекулы и способствующих формированию её уникальной конфигурации.
Разнообразные экспериментальные данные демонстрируют, что даже небольшие изменения в концентрации гидрофобных остатков могут значительно влиять на стабильность образования и функционирование белков. Увеличение количества гидрофобных взаимодействий часто ведет к повышению термостабильности, в то время как их дефицит может привести к неправильным сворачиваниям и возникновению заболеваний, таких как миелопатия или альцгеймер.
Стимулирование гидрофобных взаимодействий при дизайне новых молекулярных конструкций и лекарственных средств может обеспечить создание более эффективных терапевтических агентов. Оптимизация этих взаимодействий с помощью «молекулярного инжиниринга» открывает новые горизонты для целевой доставки и активации биологически активных соединений внутри клеток.
Таким образом, гидрофобные взаимодействия не только имеют большое значение для нормального функционирования белков, но и оказывают влияние на инновационные подходы в биотехнологии и медицине, что открывает широкий спектр возможностей для будущих исследований и разработок.
Кооперативные эффекты дофамина и адреналина
Взаимодействие между дофаминовыми и адреналиновыми молекулами формирует значительное влияние на физиологические процессы. Эти нейромедиаторы играют ключевую роль в регуляции различных систем организма, включая нервную и эндокринную. Установлено, что совместное действие адреналина и дофамина обеспечивает синергетический эффект, способствуя повышению тонуса и уровня энергии.
Отношения между дофаминовыми и адреналиновыми доменами имеют природу кооперативности, где связывание одного типа молекул способствует изменению конформаций и активности других. Например, возбуждающее действие адреналина может усиливать выделение дофамина в определённых участках мозга, что приводит к улучшению когнитивной функции и мотивации.
Одной из важных характеристик взаимодействия является их способность к обратной связи. Высокий уровень дофамина может подавлять секрецию адреналина в ответ на стресс, что демонстрирует сложность эндокринной регуляции. Исследования показывают, что баланс между этими двумя соединениями влияет на эмоциональное состояние и уровень стресса, что имеет значение для диагностики и лечения различных психологических расстройств.
В клинической практике наблюдается, что применение препаратов, воздействующих на дофаминовую и адреналиновую системы, может использоваться для корректировки состояния пациентов с депрессией или тревожными расстройствами. Понимание кооперативных эффектов этих нейромедиаторов открывает новые горизонты в психофармакологии и психотерапии.
Необходимы дальнейшие исследования для изучения системных эффектов параллельного воздействия адреналина и дофамина, что может привести к созданию более целевых методов борьбы с неврологическими и психическими расстройствами. Научное внимание к данным взаимодействиям может создать основу для новых терапевтических стратегий, направленных на улучшение качества жизни пациентов.
Влияние ионных взаимодействий на пространственную конфигурацию белков
Ионные взаимодействия играют значительную роль в формировании компоновки макромолекул, поскольку они обеспечивают стабильность и функциональность молекул. Атомы с положительным зарядом (катоны) и атомы с отрицательным зарядом (анионы) взаимодействуют между собой, образуя ионные пары, которые влияют на конформацию пептидных цепей.
Среди наиболее важных ионных взаимодействий стоит выделить водородные связи и соли, которые способствуют образованию специфических конформеров. Эти связи могут формироваться между кислородом и водородом, а также между разными функциональными группами на белковой цепи. Например, связи между карбоксильными группами и аминогруппами способствуют созданию структурных мотивов, таких как α-спирали и β-слои.
| Тип взаимодействия | Примеры | Влияние на конфигурацию |
|---|---|---|
| Катионные связи | Лизин – аспартат | Устойчивость третичных структур |
| Анионные связи | Глутамат – аргинин | Формирование доменов |
| Водородные связи | Сериновая и тирозиновая группы | Обеспечение гибкости и динамичности |
Использование различных ионных взаимодействий позволяет белковым молекулам адаптироваться к изменениям внешней среды, таких как pH и температура. Это открывает возможности для применения в биотехнологии, где оптимизация процессов с использованием ионных взаимодействий может привести к созданию более эффективных ферментов и терапевтических агентов.
В лабораторной практике моделирование ионных взаимодействий может служить инструментом для предсказания поведения белковых молекул, а также для разработки новых лекарств. Изучение ионных взаимодействий говорит о глубоком понимании механизмов, с помощью которых белковые молекулы сохраняют свою функциональность при изменяющихся условиях.
Значение дисульфидных связей в формировании окончательной структуры
Дисульфидные связи представляют собой ковалентные соединения между двумя атомами серы, образующимися в результате окисления тиоловых групп цистеина. Эти связи обладают ключевой ролью в стабильности и функциональности молекул белковых соединений.
Формирование дисульфидных мостиков происходит в условиях окислительной среды, что часто наблюдается в эндоплазматическом ретикулуме клеток. Они способствуют скреплению различных фрагментов полипептидных цепей, что обеспечивает необходимую компоновку и целостность молекулы. Без таких связей многие молекулы теряли бы свою устойчивость и не могли бы выполнять свои биологические обязанности.
- Стабилизация трехмерной конфигурации: Дисульфидные мостики формируют прочные связи, которые удерживают элементы в заданной геометрии, особенно в условиях изменений окружающей среды.
- Устойчивость к денатурации: Белки с дисульфидными связями чаще сохраняют свою активность при высоких температурах и экстремальных pH.
- Регуляция функции: Некоторые молекулы могут изменять свою активность в зависимости от состояния дисульфидных связей; их редукция и окисление служат механизмами контроля.
Примеры белков с разнообразными формами в живых организмах
Коллаген представляет собой один из наиболее распространенных компонентов соединительных тканей. Его структура обеспечивает прочность и эластичность, что делает его ключевым для кожи, сухожилий и хрящей.
Миоглобин, содержащийся в мышцах, выполняет функцию хранения кислорода. Его уникальная компоновка позволяет эффективно связывать и высвобождать молекулы кислорода, что критически важно для мышечной активности.
Антитела, такие как IgG, имеют сложную геометрию, что позволяет им специфически связываться с антигенами. Это явление обеспечивает защиту организма от патогенов, играя важную роль в иммунной реакции.
Кератин встречается в волосах, ногтях и наружном слое кожи. Благодаря своей прочности, этот компонент обеспечивает защиту от механических повреждений и агрессивных факторов окружающей среды.
Амилаза отвечает за расщепление углеводов в пищеварительном тракте. Она демонстрирует уникальную конфигурацию, которая способствует правильному взаимодействию с субстратами и обеспечению эффективного переваривания пищи.
Фермент лактаза, необходимый для расщепления лактозы, имеет специфическую форму, что позволяет ему связываться только с данным сахаром, предотвращая дискомфорт у людей с непереносимостью лактозы.
Протеин GFP (зеленый флуоресцентный белок) открывает новые горизонты в биологии и медицине благодаря своей яркой флуоресценции. Эта способность позволяет использовать GFP как маркер в исследованиях клеточных процессов.
Хемоглобин, присутствующий в красных кровяных клетках, отвечает за перенос кислорода. Его структура адаптирована для эффективной загрузки и выгрузки кислорода, что жизненно важно для метаболических процессов организма.
Методы определения третьей конструкции: преимущества и ограничения
Определение пространственной конфигурации молекулы – ключевая задача в биохимии. Разнообразные подходы помогают установить 3D-организацию сложных молекул, каждая из которых обладает своими сильными и слабыми сторонами.
- Рентгеновская кристаллография
- Преимущества: высокое разрешение (до атомного уровня); широко применяется для структур больших молекул.
- Ограничения: требует кристаллизованных образцов, что не всегда возможно; может изменять конфигурацию при кристаллизации.
- Ядерный магнитный резонанс (ЯМР)
- Преимущества: исследование белков в водных растворах, что приближает к естественным условиям; позволяет наблюдать динамику молекул.
- Ограничения: большие молекулы сложно анализировать; требует высоких концентраций образца.
- Крио-электронная микроскопия (Крио-ЭМ)
- Преимущества: не требует кристаллизации, что позволяет изучать как стабильные, так и лабильные молекулы; даёт возможность получать изображения крупномасштабных комплексов.
- Ограничения: разрешение ниже, чем у рентгеновской кристаллографии; обработка данных требует много времени.
- Флуоресцентная спектроскопия
- Преимущества: возможность изучения взаимодействия молекул в реальном времени; высокая чувствительность.
- Ограничения: зависит от наличия подходящих флуоресцентных меток; ограничения по пространственному разрешению.
- Молекулярное моделирование
- Преимущества: позволяет предсказывать структуры на основе существующих данных; полезно для исследования взаимодействий между молекулами.
- Ограничения: требует точных начальных данных и правильных моделей; может давать не всегда достоверные результаты.
Комбинирование нескольких методов часто приводит к более полному и точному пониманию молекул. Научный подход к изучению помогает преодолевать ограничения каждого из заданных методов, открывая новые горизонты в исследовании сложных систем. Выбор правильного метода зависит от специфики исследуемой молекулы и поставленных задач. От правильной комбинации зависит успешность дальнейшего анализа.
Изменения третичной структуры при патологиях и их биологические последствия
Нарушения трехмерной конфигурации полипептидных цепей могут приводить к различным заболеваниям. Изменения в молекулярной форме означают, что форма белка уже не соответствует его функциональной роли, что вызывает клинические проявления.
Одним из примеров таких изменений является болезнь Альцгеймера, связанную с агрегацией бета-амилоидных пептидов. Ненормально свернутые молекулы накапливаются в нейронах, утрачивая свои нормы функционирования, что ведет к когнитивным нарушениям.
Другой пример – муковисцидоз, при котором ген CFTR, отвечающий за транспорт ионов хлора, теряет свою работоспособность. Изменение конфигурации приводит к блокировке транспортных функций, вызывая накопление слизи в легких и нарушая дыхательные процессы.
- Миастения гравис: Дефекты белков, участвующих в передаче нервных импульсов, приводят к снижению мышечной силы.
- Сердечная недостаточность: Изменение свойств тропонинов может вызвать проблемы с сократимостью сердца.
- Идиопатический легочный фиброз: Аномалии в белках внеклеточного матрикса приводят к замене легочной ткани на фиброзные участки.
Функциональные последствия нарушений форм могут быть разнообразными. Часто это проявляется в слабости, нарушениях обмена веществ или даже в раковых заболеваниях. Применение технологии генной терапии и новых составов, способствующих восстановлению нормальной формы, является перспективным направлением в лечении.
Мониторинг изменений форм может помочь в ранней диагностике и выборе курса терапии. Важно учитывать, что каждое изменение может вызывать множественные эффекты, требующие мультидисциплинарного подхода для решения проблемы.
Перспективы применения пространственных форм белков в биотехнологии
Совершенствование технологии создания молекул с специфическими свойствами открывает новые горизонты в области биотехнологии. Применение пространственных форм, обладающих уникальными активными участками, может стать основой для разработки новых биокатов.
Направление, связанное с закономерностями связывания молекул, становится особенно актуальным. Конструирование белковых молекул с настраиваемыми сайтами связывания позволит создавать высокочувствительные биосенсоры. Например, использование антител с измененными формами может значительно улучшить специфичность и чувствительность анализа.
Также можно отметить потенциал в области терапевтических средств. Генноинженерные молекулы, имеющие тщательно спроектированные конфигурации, уже демонстрируют свою эффективность в лечении различных заболеваний, особенно в онкологии. Упаковка противораковых агентов в новые носители позволяет целенаправленно доставлять лекарства в пораженные клетки, минимизируя побочные эффекты.
Кроме того, изучение белковых активаторов и ингибиторов предоставляет возможность для создания целенаправленных терапий. Модификация пространственных форм делает их идеальными кандидатами в качестве препаратов для лечения заболеваний, связанных с нарушениями метаболизма.
Технологии CRISPR и аналогичные методы редактирования генома стали важными инструментами в доработке белков. Ожидается, что дальнейшие изучения этих молекул приведут к разработке новых подходов в создании генетически модифицированных организмов, что снижает затраты на производство и увеличивает эффективность сельского хозяйства.
В области экологии и охраны окружающей среды создание белков с определенными свойствами сможет помочь в биоремедиации и очистке воды. Разработка молекул, способных связываться с токсинами и тяжелыми металлами, может привести к значительному улучшению качества природной среды.
Таким образом, использование пространственных форм молекул в различных областях открывает новые пути для инвестиций и научных исследований, способствуя решению актуальных проблем современности.