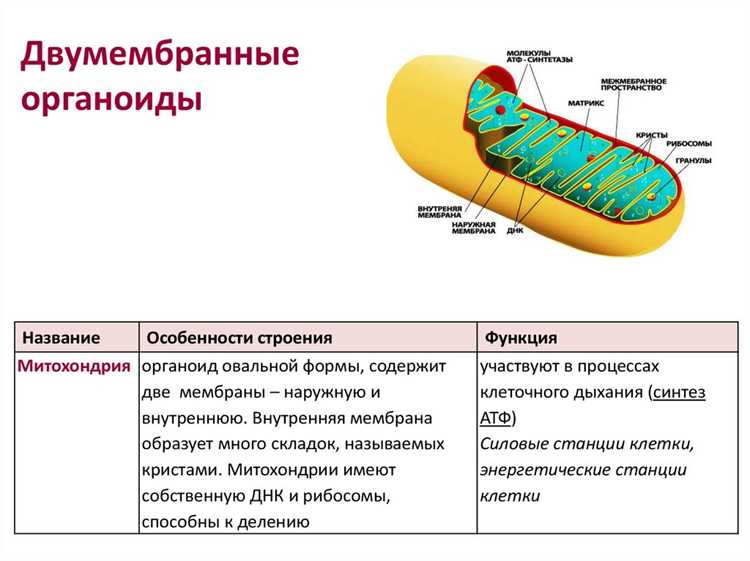
Энергетические центры клеток не просто обеспечивают необходимую для жизни силу, но и участвуют в регулировании множества других биохимических процессов. Каждая из этих миниатюрных структур занимается синтезом АТФ – молекулы, которая служит основным источником энергии для многих клеточных реакций. Количество этих органелл в различных типах клеток может варьироваться в зависимости от уровня их активности и потребности в энергии.
Более того, организмы используют эти структуры как механизмы контроля метаболизма. Они помогают в поддержании баланса между анаболическими и катаболическими реакциями, позволяя клетке адаптироваться к изменяющимся условиям окружающей среды. Наличие специфических белков и ферментов в этих органеллах способствует так называемому окислительному фосфорилированию, что является ключевым моментом в получении энергии из питательных веществ.
Также стоит отметить их участие в процессах апоптоза – программируемой клеточной гибели, которая важна для поддержания гомеостаза. Когда клетка устаревает или повреждается, именно эти структуры инициируют сигналы, запускающие соответствующие молекулярные каскады. Этим они играют критически важную роль в развитии и регенерации тканей, обеспечивая очистку организма от ненужных или дефектных клеток.
Роль митохондрий в энергетическом обмене клеток
Каждый из пяти основных комплексов дыхательной цепи играет свою роль в передаче электронов. Комплекс I (NADH-дегидрогеназа) и Комплекс II (сукцинат-дегидрогеназа) переносят электроны, которые затем через Комплекс III и Комплекс IV приводит к образованию простагландинов. Это способствует созданию протонного градиента, который используется АТФ-синтазой для образования АТФ из АДФ и фосфата.
Продуцирование АТФ происходит не только на уровне митохондрий, но и напрямую зависит от метаболизма питательных веществ. Гликолиз, протекающий в цитозоле, обеспечивает ключевые молекулы, такие как пируват, которые затем направляются внутрь органеллы. Оксидативный метаболизм таких субстратов, как пируват и жирные кислоты, приводит к значительно более высокому выходу энергии по сравнению с анаэробным расщеплением глюкозы.
Корректная работа этих клеточных структурах также важна для поддержания клеточного гомеостаза. Отказ в их функционировании может вызвать накопление неблагоприятных промежуточных соединений и привести к окислительному стрессу. Поэтому поддержание здорового баланса в этом значении требует наличия антиоксидантов, таких как глутатион и витамин Е.
Командная работа разных категорий клеток требует от них высокого уровня метаболической адаптивности. В ситуациях, где требуется непременная энергетическая поддержка (например, во время физической активности), активизируется процесс приоритизации производства АТФ. Это происходит за счет увеличения активности кислородного дыхания и увеличения числа органелл в клетках. Например, мышечные клетки демонстрируют значительную гипертрофию митохондрий при регулярных физических нагрузки.
Существуют различные подходы к исследованиям этих структур, включая применение препаратов, способствующих улучшению функционирования. Одним из таких направлений является использование коэнзима Q10, который способствует стимулированию процессов молекулярной кислородной аэрации и защиты от окислительного повреждения.
Как митохондрии участвуют в апоптозе?
Апоптоз представляет собой программированную гибель клеток, необходимую для поддержания гомеостаза и удаления поврежденных элементов из организма. Энергетические структуры играют ключевую роль в этом процессе, осуществляя множество функций, связанных с индукцией и регуляцией апоптоза.
Первоначально, выход проапоптозных белков из рассматриваемых структур, таких как цитохром c, инициирует каскад событий, приводящих к активизации каспаз. Эти ферменты, действуя на субстраты, обладают способностью вызывать разрушение клеточных компонентов и запускать последовательность, приводящую к гибели клетки.
В дополнение, насыщение клеточного окружения реактивными формами кислорода (РС) также вызывает стресс, который может служить триггером для запуска программируемой клеточной смерти. Складывающиеся условия, такие как повреждение ДНК или нарушение метаболизма, могут привести к активации белка p53, который действует как регулятор, способствующий активации механизма апоптоза.
Мембранные потенциалы и проницаемость внешних оболочек играют значительную роль в контроле над процессами, связанными с клеточной смертью. Изменения в этих параметрах могут привести к дестабилизации внутренней среды, что ещё больше содействует высвобождению проапоптозных факторов.
Также стоит отметить, что уровень взаимодействия между белками Bcl-2 и Bax значительно влияет на результат: соотношение этих молекул определяет, будет ли клетка выживать или погибнет. Дизбаланс в их активности может привести к аллергическим, аутоиммунным или канцерогенным состояниям.
Понимание механизмов участия этих структур в программируемой клеточной смерти позволяет разрабатывать новые терапевтические подходы, направленные на подавление или стимуляцию апоптоза в различных заболеваниях, включая рак и нейродегенеративные расстройства.
Обеспечение клеток АТФ: механизмы и процессы
АТФ – главный энергетический носитель в живых организмах. Он синтезируется в клетках через несколько ключевых этапов, включая гликолиз, цикл Кребса и окислительное фосфорилирование.
Основные механизмы синтеза АТФ включают:
- Гликолиз: Процесс, происходящий в цитозоле, где одна молекула глюкозы расщепляется на две молекулы пирувата, образуя 2 молекулы АТФ и 2 молекулы NADH.
- Цикл Кребса: Пируват переходит в митохондрии, где проходит через серию реакций, в результате которых образуются NADH и FADH2, а также выделяется углекислый газ.
- Окислительное фосфорилирование: Процесс, при котором электроны из NADH и FADH2 передаются через электронно-транспортную цепь, находящуюся в внутренней мембране, приводя к синтезу АТФ и потреблению кислорода.
Для оптимального синтеза АТФ клеткам необходимы:
- Энергетические субстраты: Глюкоза, жирные кислоты и аминокислоты обеспечивают топливо для метаболических реакций.
- Кислород: Необходим для окислительного фосфорилирования, особенно в тканях с высоким уровнем метаболической активности.
- Микроэлементы: Витамины и минералы, такие как магний и некоторые витамины группы B, играют ключевую роль в метаболизме и ферментативных реакциях.
Нарушения в механизмах выработки АТФ могут приводить к различным заболеваниям, включая митохондриальные расстройства и возрастные болезни.
Контроль уровня АТФ в клетках возможен через:
- Диету: Оптимальное потребление углеводов, белков и жиров.
- Физическую активность: Регулярные тренировки увеличивают потребление кислорода и усиливают энергетический обмен.
- Антиоксидантную защиту: Защита от окислительного стресса улучшает общую метаболическую активность.
Поддержание баланса в метаболических процессах способствует эффективному производству АТФ и общему состоянию здоровья организма.
Влияние митохондрий на уровень реактивных форм кислорода
Производство реактивных форм кислорода (РФК) в пределах органелл имеет прямое отношение к энергетическому обмену. Основной путь генерации этих соединений осуществляется во время окислительного фосфорилирования, особенно на уровне комплекса I и III цепи переносчиков электронов. В нормальных условиях уровень РФК поддерживается на минимальном уровне благодаря системе антиоксидантной защиты, которая включает глутатион, супероксиддисмутазу и каталазу.
При увеличении энергетических потребностей или нарушениях в метаболизме может произойти избыток РФК. Это вызывает окислительный стресс, который ведет к повреждению белков, липидов и ДНК, что напрямую связанных с развитием различных заболеваний, включая нейродегенеративные и сердечно-сосудистые расстройства. Важно контролировать уровень этих соединений с помощью антиоксидантов, таких как витамины C и E, чтобы минимизировать повреждение клеток.
Поддержание баланса между образованием и разложением РФК имеет значение для нормального функционирования. К примеру, учитывая роль РФК в клеточной сигнализации, небольшие их дозы могут быть необходимы для активации определенных путей, включая пролиферацию и адаптацию к стрессовым условиям. В этом контексте, аэробные тренировки могут способствовать улучшению антиоксидантной системы, что ведет к уменьшению окислительного стресса.
Патологии, связанные с избытком РФК, можно частично контролировать через изменения в образе жизни. Регулярная физическая активность, сбалансированное питание, богатое антиоксидантами, а также минимизация воздействия токсинов будут способствовать снижению уровня окислительного стресса. Также перспективно использование добавок, направленных на снижение образования РФК в органеллах, таких как пируват и альфа-кетоглутарат, которые помогают улучшить энергетический метаболизм и уменьшить окислительное повреждение.
Митохондрии и регуляция клеточного метаболизма
Энергетические станции клеток играют ключевую роль в поддержании обмена веществ. Они отвечают за выработку АТФ через окислительное фосфорилирование и обеспечивают клетки энергией, необходимой для различных биохимических реакций.
Процессы митохондриального дыхания зависят от окисления пищи, в частности, глюкозы и жирных кислот. Конверсия этих макронутриентов в АТФ осуществляется посредством цепи переноса электрона, где электроны передаются от доноров на акцепторы. Одним из важнейших акцепторов является кислород, что подчеркивает важность кислородного состояния для метаболизма.
Многочисленные факторы влияют на управление энергетическим состоянием. Например, уровни внутреклеточных метаболитов, таких как АТФ, АДФ и солей кальция, напрямую меняют активность ключевых ферментов метаболических путей. Высокое содержание АТФ сигнализирует о достаточной энергии, при этом низкий уровень активирует ферменты, ведущие к распаду глюкозы или жиров.
Помимо этого, модуляция генов, кодирующих жизненно важные белки в этой области, типа цитохромов или транспортных белков, также существенно сказывается на метаболических функциях. Гены, связанные с биогенезом, активируются в ответ на метаболические изменения и стрессовые условия, что, в свою очередь, перераспределяет ресурсы, поддерживая здоровье клетки.
Не стоит забывать о влиянии окислительного стресса, который может нарушить баланс между образованием и нейтрализацией свободных радикалов. Это может вызвать изменения в метаболизме, замедляющие протекание клеточных реакций. Применение антиоксидантных веществ может помочь сбалансировать этот процесс.
Изменения в активности энергетических станций могут служить маркером патологий. Например, в случаях диабета или сердечно-сосудистых заболеваний наблюдаются нарушения в продуктивности и динамике обмена веществ. Исследования показывают, что нормализация процессов клеточной энергетики может представлять собой перспективный путь лечения этих состояний.
Отслеживание и оптимизация метаболических путей может быть полезен для улучшения физической работоспособности и общего состояния здоровья. Введение диетических коррекций, таких как увеличение потребления здоровых жиров и углеводов с низким гликемическим индексом, может поддерживать и повышать производительность энергетических систем в клетках.
Значение митохондриальной ДНК в клеточных функциях
ДНК, находящаяся в органеллах, контролирует синтез белков, необходимых для основной энергетической деятельности. В отличие от ядерной ДНК, этот генетический материал имеет уникальную структуру и порой кардинально отличается от хромосомного набора. Основная роль данного ДНК заключается в кодировании компонентов дыхательной цепи, которая обеспечивает АТФ – главный энергетический носитель.
Кодируемые гены играют ключевую роль в поддержании метаболизма. Отклонения в их последовательностях могут приводить к неправильно функционирующим белкам. Это, в свою очередь, может вызвать нарушения в энергопроизводстве и вызвать различные заболевания. Анализ митохондриальных генов обладает значением в диагностике множества наследственных расстройств.
| Функция | Роль |
|---|---|
| Синтез белков | Необходим для функционирования дыхательной цепи. |
| Регуляция энергетического обмена | Контролирует уровень АТФ в клетках. |
| Участие в апоптозе | Медирует процессы программируемой клеточной смерти. |
Кроме того, митохондриальная ДНК подвержена мутациям, которые могут накапливаться с возрастом. Эти изменения могут влиять на повседневную жизнедеятельность особи, особенно на устойчивость к стрессовым факторам. Данные мутации играют роль в старении и патологиях, таких как болезнь Альцгеймера или Паркинсона.
Современные методы исследования, включающие секвенирование и технологии CRISPR, предоставляют новые возможности для изучения митохондриальной генетики. Понимание их роли в патогенезе diseases может привести к созданию новых терапевтических стратегий, направленных на профилактику и лечение различных расстройств, связанных с энергетическим метаболизмом.
Сигнальные пути, связанные с митохондриями
Основные сигнальные каскады, ассоциированные с этими органеллами, включают:
- AMPK (аденозинмонофосфат-активируемая протеинкиназа):
- Активируется при низком уровне АТФ и высоким уровне АМФ.
- Регулирует энергетический метаболизм, способствуя окислению жирных кислот и гликолизу.
- mTOR (мишень рапамицина у млекопитающих):
- Участвует в контроле клеточного роста и синтеза белка.
- Связывается с доступностью питательных веществ и уровнем энергии.
- NF-kB (ядерный фактор каппа B):
- Активируется в ответ на стресс и воспаление.
- Регулирует экспрессию генов, связанных с выживанием клеток.
- JNK (киназа, активируемая стрессом):
- Участвует в ответе на стресс и может вызывать апоптоз.
- Регулирует клеточный цикл и метаболизм.
Сигнальные молекулы, такие как цитокины, могут активировать эти пути, что приводит к изменению клетечного метаболизма в ответ на различные стимулы. Это открывает возможности для разработки терапевтических стратегий при метаболических заболеваниях и раке.
Нарушения в таких каскадах могут привести к патологиям, таким как диабет, сердечно-сосудистые болезни и нейродегенеративные расстройства. Разработка препаратов, направленных на корректировку этих сигнальных маршрутов, представляет собой многообещающую область исследований.
Клинические испытания показывают, что модификация активности регуляторов, таких как AMPK и mTOR, может улучшить метаболические параметры и замедлить прогрессирование заболеваний. Таким образом, акцент на исследование влияния альтернативных метаболических путей откроет новые горизонты для инновационной медицины.
Митохондрии и клеточный стресс: адаптация и защита
Критическое значение энергии для клеток делает органеллы центральными игроками в реакциях на неблагоприятные условия. Они участвуют в регуляции уровня реактивных форм кислорода (РФК), образующихся при окислительном метаболизме. Увеличение концентрации РФК запускает окислительный стресс, что может привести к повреждению белков, липидов и ДНК.
В условиях стресса многие структуры переходят в состояние предохранения. Это проявляется в изменении активности ферментов, повышении производительности антиоксидантных систем и активации молекул шокового белка. Такие реакции помогают снизить уровень токсичных метаболитов и сохранить целостность клеток.
Процессы аутопагии также получают активизацию. Этот механизм позволяет удалять поврежденные органеллы и белки, что способствует поддержанию гомеостаза внутри клеток. Современные исследования показывают, что нарушенная аутопагия может быть связано с патогенезом различных заболеваний, включая нейродегенеративные расстройства и рак.
Необходимость поддержания энергетического баланса в условиях стресса подчеркивает важность альтернативных метаболических путей. Увеличение β-окисления жирных кислот, например, помогает восполнить энергетические запасы в периоды нехватки глюкозы. Это переключение метаболизма является важным адаптивным механизмом, позволяющим клеткам выживать.
Разработка терапий, направленных на поддержание функций органелл, может стать терапевтической стратегией для лечения заболеваний, вызванных окислительным стрессом. Исследования показывают, что соединения, способствующие повышению активности молекул, способствующих защите клеток, могут помочь в восстановлении их функций, особенно в условиях нагрузок.
Влияние митохондрий на старение клеток
Генерация АТФ напрямую зависит от состояния мембранной функции. Со снижением этого показателя происходит уменьшение энергии, что негативно сказывается на обменных процессах. В результате клетки теряют способность к делению и восстановлению. С возрастом коммутирующие протеазы и другие ферменты, ответственные за очистку, показывают снижение активности, что приводит к замедлению адаптивных механизмов.
Недавно стало известно, что митохондрии могут участвовать в секреции провоспалительных молекул. Этот процесс способствует хронизации воспалительных реакций, ассоциированных со старением. Такой эффект очевиден при исследовании возрастных заболеваний, таких как диабет и болезни сердца.
Рекомендации по улучшению работы митохондрий включают:
| Метод | Описание |
|---|---|
| Физическая активность | Регулярные упражнения помогают повысить биогенез митохондрий и улучшить их функцию. |
| Сбалансированное питание | Употребление антиоксидантов, таких как витамины C и E, помогает снизить оксидативный стресс. |
| Контроль стресса | Методы релаксации оказывают положительное влияние на общее состояние, снижая уровень воспалительных молекул. |
| Сон | Полноценный отдых способствует восстановлению и поддержанию энергетического баланса в клетках. |
Таким образом, именно активность клеточных структур определяет устойчивость к возрастным изменениям. Поддержание оптимального состояния энергетических станций является важным аспектом здравоохранения и долголетия.
Перспективы терапии заболеваний с дисфункцией органелл
Современные методы лечения заболеваний, связанных с нарушениями в работе органелл, показывают многообещающие результаты. Одна из ключевых стратегий на сегодняшний день заключается в использовании специфических веществ для улучшения энергетического обмена и восстановления нормальной функции клеток.
- Метаболические препараты: Такие вещества, как пируват и ацетил-L-карнитин, способны увеличивать уровень энергии и способствовать процессам восстановления.
- Антиоксидантная терапия: Использование антиоксидантов, таких как кофермент Q10 и альфа-липоевая кислота, помогает уменьшить оксидативный стресс и улучшить общее состояние клеток.
- Генетическая терапия: Применение технологий редактирования генома, таких как CRISPR, демонстрирует потенциал в коррекции мутаций, приводящих к дисфункции органелл.
Исследования показывают, что фармакологическая коррекция может быть комбинирована с физической активностью для достижения наилучших результатов. Упражнения стимулируют адаптацию тканей и помогают улучшить обмен веществ.
- Применение специальных диет, богатых омега-3 жирными кислотами, предрасположено к восстановлению нормальной работы клеточных структур.
- Поддержание оптимального уровня витаминов, таких как витамин D и B-комплекс, способствует улучшению функций клеточных компонентов.
Перспективы лечения подразумевают индивидуальный подход, учитывающий генетические и метаболические особенности пациента, что позволит создать более целенаправленные и безопасные методы воздействия на заболевания.
Научные находки в области клеточной биологии создают предпосылки для дальнейших исследований в этой области. С каждым годом появляются новые данные о механизмах заболеваний, что открывает новые горизонты для создания инновационных терапий.