Протеины представляют собой сложные молекулы, состоящие из цепочек аминокислот, которые играют центральную роль в функционировании организма. Известно, что на человеческий организм приходится двадцать стандартных аминокислот, каждая из которых уникальна по своему химическому строению и функциональности. Из этих двадцати девять являются незаменимыми, что означает, что их поступление с пищей необходимо для поддержания здоровья.
Аминокислоты, входящие в состав структур, таких как коллаген и кератин, способствуют поддержанию целостности тканей и росту мышечной массы. Они взаимодействуют друг с другом в определенных пропорциях, что формирует уникальные структуры, характерные для различных протеинов. К примеру, лейцин, валин и изолейцин важны для восстановления мышечных волокон после перегрузок.
При выборе источников протеинов стоит обратить внимание на продукты, которые содержат полные молекулы с высоким содержанием незаменимых аминокислот. Мясо, рыба, яйца, а также растительные альтернативы, такие как бобовые и соя, могут стать основными элементами сбалансированного рациона. Факторы, влияющие на усвоение этих соединений, включают время приема пищи и сочетание с другими продуктами.
Структурные особенности аминокислот
Аминокислоты представляют собой основные единицы, из которых формируются длинноцепочечные молекулы. Каждая из них состоит из центрального атома углерода, к которому прикреплены четыре группы: аминогруппа (NH2), карбоксильная группа (COOH), водородный атом и радикал, определяющий специфические свойства аминокислоты.
Функциональные группы на радикалах создают значительное разнообразие свойств. Полярные радикалы, такие как гидроксильная или амидная группы, указывают на способность образовывать водородные связи, тогда как неполярные радикалы, например, состоящие из углеводородных цепей, характеризуются гидрофобностью и могут влиять на пространственную конфигурацию молекул.
Степень и характер интеракций между радикалами аминокислот определяет третичную и четвертичную структуры сложных молекул. Например, нековалентные взаимодействия, такие как ионные связи, водородные связи и Ван дер Ваальсовы силы, играют важную роль в стабилизации белковых структур. Ковалентные связи, такие как дисульфидные мостики, также вносят в значительный вклад в прочность двухмерных и многомерных форм.
Аминокислоты могут варьироваться по своей способности к образованию солей и взаимодействию с водой. Наличие кислых или основных радикалов определяет поведение молекулы в условиях различных pH. Миноритарные аминокислоты, такие как селенометионин, могут вносить дополнительные биологические функции благодаря специфическим свойствам своих структур.
Изучение пространственной конфигурации аминокислот и взаимодействий между ними даёт понимание процессов, происходящих в клетках. Это знание необходимо для разработки биотехнологий и медицинских препаратов, направленных на улучшение функций живых организмов.
Роль пептидных связей в формировании белка
Пептидные связи представляют собой химическую связь между аминокислотами, которая играет ключевую роль в структуре и функции полипептидных цепей. Эти связи образуются через реакцию конденсации, в процессе которой образуется водяная молекула. В результате, две аминокислоты соединяются, формируя пептид.
Каждая пептидная связь является результатом взаимодействия аминогруппы одной аминокислоты и карбоксильной группы другой. Это соединение приводит к образованию цепочки, которая может иметь различные длины и последовательности, определяющие физико-химические свойства конечного продукта. Пептидные связи являются стабильными под физиологических условий, что делает их надежными структурными элементами.
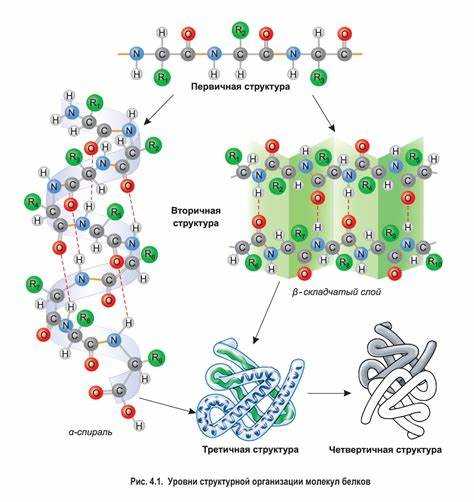
Структура, формируемая благодаря пептидным связям, может принимать различные конфигурации. Она может быть линейной или закрученной, что и определяет функциональные характеристики. Спирали и складки, образующиеся в результате взаимодействия пептидных связей, обеспечивают поддержание специфической трёхмерной формы, необходимой для выполнения биологических функций.
Аминокислоты, соединённые пептидными связями, могут подвергаться различным модификациям, что далее влияет на стабильность и активность конечного соединения. Например, фосфорилирование или гликозилирование могут изменять свойства и функции молекулы. Кроме того, пептидные связи способны влиять на взаимодействие с другими молекулами в клетке, что важно для процессов сигнализации и регуляции.
Классификация аминокислот: незаменимые и заменимые
Незаменимые соединения не могут синтезироваться организмом и должны поступать с пищей. К таким относятся: лейцин, изолейцин, валин, лизин, метионин, триптофан, фенилаланин и треонин. Эти вещества необходимы для роста, восстановления тканей и поддержки иммунной системы. Для полноценного функционирования важно включать в рацион продукты, богатые этими аминокислотами, такие как мясо, рыба, яйца и молочные изделия.
Заменимые аминокислоты организм может сам вырабатывать, но их также можно получать из пищи. К ним относятся: аланин, аспарагин, глицин, глутамин, серин, тирозин и цистеин. Эти соединения поддерживают обмен веществ, участвуют в синтезе нейромедиаторов и регулируют метаболические процессы. Для их поступления подойдет разнообразный рацион, включающий бобовые, орехи и злаки.
Баланс между незаменимыми и заменимыми аминокислотами важен для здоровья. Разнообразие источников пищи поможет обеспечить достаточное поступление всех видов, что в свою очередь позволит поддерживать оптимальное состояние организма и улучшать общую работоспособность.
Влияние белка на метаболизм организма
Протеин играет ключевую роль в метаболических процессах, обеспечивая организм необходимыми аминокислотами, которые участвуют в синтезе гормонов, ферментов и клеточных структур. Способствуя формированию мышечной массы, он также повышает уровень базального обмена, позволяя сжигать больше калорий даже в состоянии покоя.
При потреблении высококачественного источника протеина отмечается увеличение термогенеза, что ведет к более высокому расходу энергии в процессе переваривания и усвоения. Это дополнительно поддерживает процессы похудения и снижение процента жира в организме.
Необходимый для синтеза молекул, участвующих в обмене веществ, он также поддерживает иммунную систему, участвуя в образовании антител. Поэтому недостаток этого компонента может ослабить защитные функции, что негативно отразится на общем состоянии здоровья.
Оптимальное распределение приёмов пищи с включением источников протеина в каждый из них помогает обеспечить более равномерный уровень сахара в крови и снизить вероятность резких колебаний энергии. Рекомендуется выбирать разновидности, которые содержат все незаменимые аминокислоты, такие как яйца, рыба, мясо и бобовые, обеспечивая организм всей необходимой питательной базой для стабильного метаболизма.
Потребление протеина после физических нагрузок также способствует восстановлению тканей мышц и улучшению результатов тренировок. Важно следить за качеством источников, предпочтительность отдавать натуральным продуктам, избегая чрезмерной обработки.
Продукты, богатые белком: что выбрать?
Выбор продуктов, содержащих высокий уровень белка, может существенно повлиять на здоровье и физическую активность. Рассмотрим наиболее подходящие варианты.
Мясо и птица. Говядина, свинина, куриное филе и индейка являются отличными источниками белковых веществ. Например, 100 грамм куриного филе содержит около 32 граммов чистого белка. Для тех, кто избегает жирного мяса, рекомендованы нежирные сорта, такие как куриная грудка.
Рыба и морепродукты. Лосось, тунец и треска содержат не только белок, но и полезные омега-3 кислоты. В 100 граммах лосося можно найти примерно 25 граммов белка. Морепродукты, такие как креветки, также богаты белковыми соединениями и низкокалорийны.
Яйца. Один из самых доступных источников. В одном яйце содержится около 6 граммов белковых веществ. Яйца можно употреблять разнообразно – вареными, жареными или в виде омлета.
Молочные продукты. Творог, йогурты и сыр также могут стать частью рациона. 100 граммов творога содержит около 18 граммов белка и высокий уровень кальция. Йогурт – не только вкусный, но и легкий способ увеличить суточную норму.
Растительные источники. Бобовые, такие как чечевица и нут, являются отличной альтернативой. Например, 100 граммов вареной чечевицы содержит 9 граммов белка. Киноа и гречка также стоит рассмотреть благодаря их высокому содержанию протеинов.
Орехи и семена. Миндаль, грецкие орехи и семена чиа могут дополнить рацион. 100 граммов миндаля содержит около 21 грамма белка. К тому же, они богаты клетчаткой и полезными жирами.
Выбор зависит от предпочтений и целей. Соблюдение баланса между животными и растительными источниками сделает рацион разнообразным и полноценным. Подходите к вопросу осознанно, учитывая индивидуальные потребности и особенности организма.
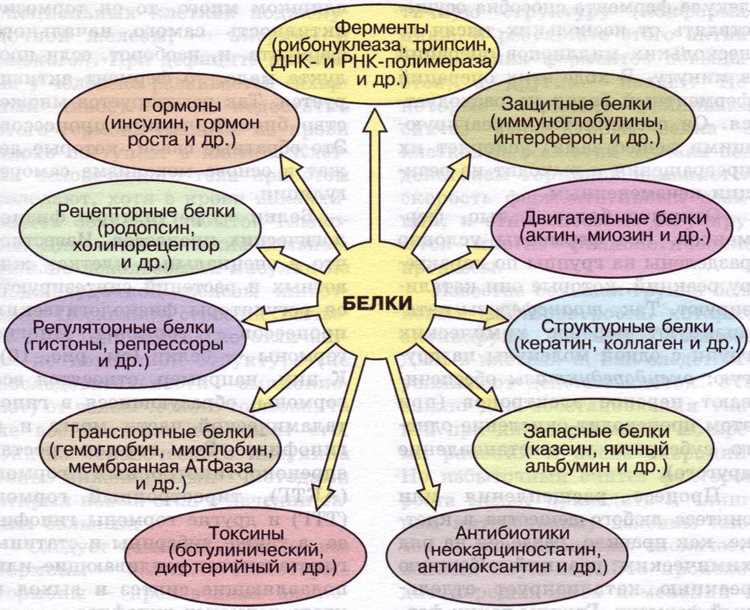
Функции белков в клеточных процессах
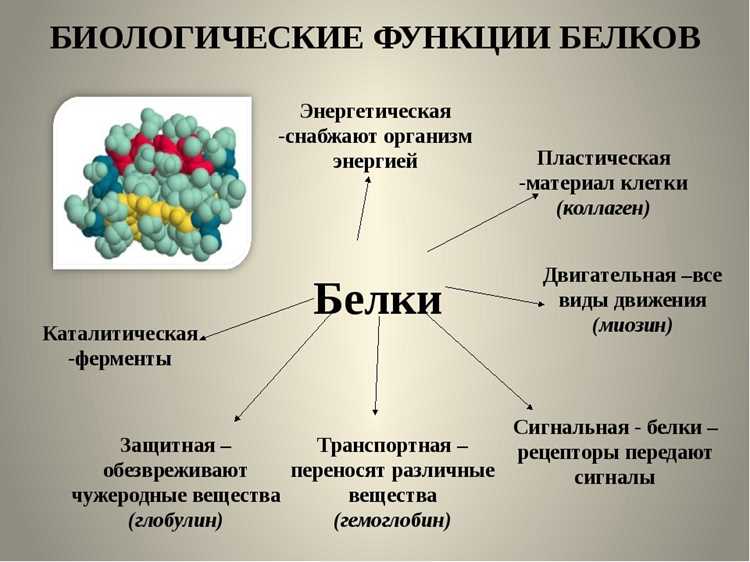
Клеточные процессы представляют собой сложные взаимодействия, в которых участвуют полипептиды. Они выполняют множество функций, воздействуя на метаболизм и регуляцию клеточных функций.
- Каталитическая активность: Многие полипептиды действуют как ферменты, ускоряющие химические реакции. Например, амилоза расщепляет углеводы, а липаза участвует в метаболизме жиров.
- Транспорт веществ: Различные структуры, такие как гемоглобин и миоглобин, обеспечивают транспорт кислорода в организме. Постоянный обмен кислорода и углекислого газа поддерживает клеточный метаболизм.
- Структурная поддержка: Белки, такие как коллаген и кератин, обеспечивают прочность тканей. Они создают каркас для клеток и органов, способствуя поддержанию формы организма.
- Регуляция: Гормоны, состоящие из полипептидов, регулируют множество процессов. Например, инсулин контролирует уровень сахара в крови, а адреналин отвечает за реакцию на стресс.
- Иммунный ответ: Имуноглобулины защищают организм от инфекций. Они распознают чуждые патогены и способствуют их нейтрализации.
- Сигнальные механизмы: Полипептиды участвуют в клеточной коммуникации, передавая сигналы между клетками. Например, рецепторы на клеточных мембранах взаимодействуют с внешними молекулами, что инициализирует ответ клетки.
Следует учитывать, что изменения в функциях полипептидов могут привести к различным заболеваниям. Поддержание оптимального уровня данных структур в организме имеет решающее значение для здоровья.
Регулярное поступление необходимых аминокислот с пищей, а также соблюдение сбалансированного рациона способствует нормальному функционированию всех клеточных процессов. Рассмотрение этих аспектов позволит более эффективно поддерживать здоровье организма.
Методы анализа белков
Определение характеристик белковых молекул требует применения различных аналитических подходов. Существуют как классические, так и современные методы, позволяющие получать качественные и количественные данные.
-
Электрофорез — один из самых распространенных способов. Этот метод использует электрическое поле для разделения макромолекул на основе их заряда и размера. Чаще всего применяется SDS-PAGE для анализа чистоты.
-
Хроматография — эффективный метод, позволяющий отделять белки по их размеру, заряду или полярности. Размерная эксклюзивная хроматография (SEC) и ионообменная хроматография широко используются для очистки.
-
Спектроскопия — применяются различные техники, такие как UV-видимая спектроскопия и ядерный магнитный резонанс (ЯМР). Эти методы позволяют изучать структуру белков на уровне состояний и взаимодействий.
При выборе метода важно учитывать задачи исследования и доступное оборудование. Некоторые анализы требуют предварительной подготовки образцов, включая денатурацию или фракционирование с использованием центрифугирования.
-
Подготовка образцов:
- Концентрация белков для повышения чувствительности анализа.
- Очистка от мешающих молекул с использованием аффинной хроматографии.
-
Выбор метода:
- Для количественного определения имеет смысл использовать ELISA.
- При необходимости изучения структуры подойдут Рентгеновская дифракция или крио-ЭМ.
Каждый метод имеет свои преимущества и ограничения, которые необходимо учитывать при планировании эксперимента. Надежные результаты зависят от тщательной калибровки и оптимизации условий. Таким образом, знание различных методик позволяет исследователям глубже понять природу и функциональность молекул.
Синтез белков: от ДНК до функциональных молекул
Процесс образования молекул, состоящих из аминокислот, начинается с ДНК, содержащей информацию о последовательности этих строительных единиц. Генетический код, записанный в нуклеотидах, определяет, какие аминокислоты будут включены в полипептидную цепь.
На первом этапе происходит транскрипция: участок ДНК разматывается, и на его основании создается молекула мРНК. Эта молекула затем покидает ядро и переходит в цитоплазму, где она будет использоваться для синтеза белков.
Следующий шаг – трансляция. МРНК связывается с рибосомой, служащей местом сборки. Рибосома считывает информацию с мРНК и переводит её в последовательность аминокислот. Каждая аминокислота доставляется специализированной транспортной РНК (тРНК), которая распознаёт кодоны на мРНК и связывает их с соответствующими аминокислотами.
Процесс продолжается, пока не завершится синтез цепи. По завершении, полипептиды требуют модификаций, таких как фосфорилирование или гликозилирование, чтобы получить активную форму. Эти изменения могут влиять на стабильность, функциональность и взаимодействие молекул с другими клеточными структурами.
Активация и работа готового продукта часто требуют взаимодействия с другими молекулами. Таким образом, завершающий этап включает в себя сборку белковых комплексов, которые могут выполнять различные функции в клетке, от катализирования химических реакций до обеспечения структурной поддержки.
Роль белков в спортивном питании и восстановлении
Спортсменам рекомендуется потреблять около 1.2-2.0 граммов протеинов на килограмм массы тела в зависимости от уровня активности и целей тренировок. Например, атлеты, занимающиеся силовыми видами спорта, должны стремиться к верхней границе этой нормы.
| Тип активности | Рекомендованное количество (г/кг массы тела) |
|---|---|
| Силовые тренировки | 1.6-2.0 |
| Выносливые тренировки | 1.2-1.4 |
| Сила + выносливость | 1.4-1.6 |
Протеиновые коктейли и другие подобные продукты могут помочь спортсменам достичь своих целей за счет легкости в усвоении и быстроты, с которой они могут быть употреблены после физической нагрузки. Комбинация углеводов и аминокислот ускоряет репарацию, а также восстанавливает запасы гликогена.
Также стоит учитывать, что различные источники спортивного питания могут отличаться по скорости усвоения. Например, сывороточный протеин усваивается быстрее, чем казеин, что делает его идеальным вариантом для употребления сразу после тренировки. Напротив, казеин можно использовать в качестве ночного белка, поскольку его усвоение происходит медленно, что обеспечивает снабжение организма аминокислотами в течение ночного отдыха.
Кроме того, важно учитывать не только количество, но и высокое качество потребляемого белка. Источники животного происхождения обеспечивают более полный аминокислотный профиль по сравнению с растительными. Однако сбалансированная диета, включающая разнообразные продукты, может обеспечить все необходимые вещества.